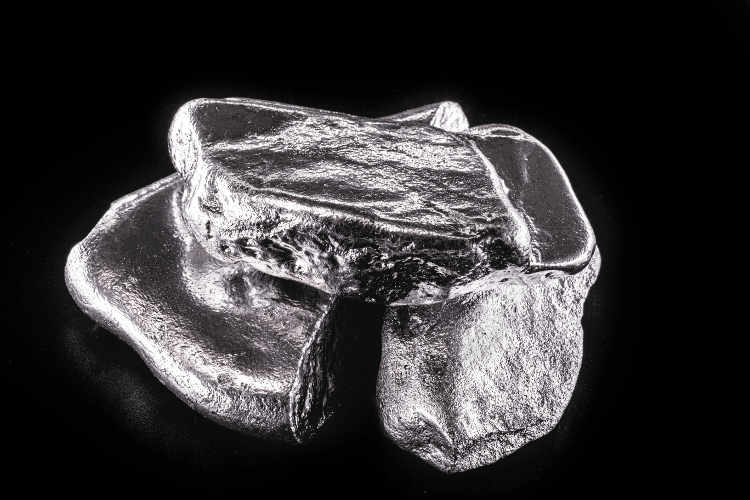
Rhodium - wertvolles Edelmetall
Rhodium findet nicht nur in Katalysatoren seine Verwendung

Rhodium gehört zu den Platingruppen-Metallen, zu welchen auch Platin und Palladium gehören. Im Vergleich zu den beiden anderen genannten Edelmetallen ist Rhodium relativ unbekannt. Ein Großteil des weltweit abgebauten Rhodiums wird in Katalysatoren verbaut.
Der Preis für Rhodium hat sich in den letzten Jahren steil nach oben entwickelt. So lag der Preis je Unze Rhodium Mitte der 2010er-Jahre noch unter 1000 Euro je Unze. Heute beträgt dieser Preis ein vielfaches und bewegt sich im fünfstelligen Eurobereich je Rhodium-Unze.
In diesem Text erhalten Sie von uns viele interessante Informationen zum Thema Rhodium zusammenfasst. Wo wird Rhodium abgebaut, was versteht sich unter rhodinierten Schmuck und welche anderen Verwendungen hat Rhodium noch?
Inhaltsverzeichnis
- Preis für Rhodium im Ankauf in Euro
- Eigenschaften von Rhodium
- Preis für Platingruppen-Metalle im Ankauf
- Daten zu Rhodium
- Preisentwicklung Edelmetalle im Vergleich (Grafik)
- Entdeckung von Rhodium
- Wofür wird Rhodium verwendet?
- Fakten zu Rhodium
- Abbau von Rhodium
- Rhodium als Sonnenenergiespeicher
- Was bedeutet rhodiniert und weitere Fragen
- Rhodium Fazit
Preis für Rhodium im Ankauf in Euro
| Rhodiumlegierung | 1 Gramm | 10 Gramm | 20 Gramm | 50 Gramm |
|---|---|---|---|---|
| 999 Rhodium | 43,15 € | 431,50 € | 863,00 € | 2.157,50 € |
| 986 Rhodium | 41,28 € | 412,80 € | 825,60 € | 2.064,00 € |
| 916 Rhodium | 31,25 € | 312,50 € | 625,00 € | 1.562,50 € |
| 900 Rhodium | 28,96 € | 289,60 € | 579,20 € | 1.448,00 € |
| 875 Rhodium | 25,38 € | 253,80 € | 507,60 € | 1.269,00 € |
| 833 Rhodium | 19,36 € | 193,60 € | 387,20 € | 968,00 € |
| 750 Rhodium | 7,47 € | 74,70 € | 149,40 € | 373,50 € |
| 585 Rhodium | 8,82 € | 88,20 € | 176,40 € | 441,00 € |
| 417 Rhodium | 9,75 € | 97,50 € | 195,00 € | 487,50 € |
| 375 Rhodium | 3,73 € | 37,30 € | 74,60 € | 186,50 € |
| 333 Rhodium | 3,05 € | 30,50 € | 61,00 € | 152,50 € |
Eigenschaften von Rhodium
Rhodium ist eines der sechs Platingruppenmetalle: Platin, Palladium, Rhodium, Osmium, Iridium und Ruthenium. Es wird auch als Edelmetall eingestuft, was bedeutet, dass es nicht so leicht mit Sauerstoff reagiert, als fantastischer Katalysator wirkt und resistent gegen Korrosion und Oxidation ist. Einige gemeinsame Eigenschaften der Platingruppenmetalle sind laut Chemie-Libretexten hohe Schmelzpunkte, allgemeine Ungiftigkeit und Beständigkeit gegen Verschleiß, Oxidation und Korrosion. Rhodium ist das Seltenste der Platingruppe und kommt nur bis zu einem Teil pro 200 Millionen in der Erdkruste vor, so Chemistry Libretexts. Rhodium hat eine geringere Dichte und einen höheren Schmelzpunkt als Platin. Laut Lenntech wird Rhodium von Luft und Wasser bis zu 1.112 Grad Fahrenheit (600 Grad Celsius) nicht angegriffen.
Preis für Platingruppen-Metalle im Ankauf
| Edelmetall | 1 Gramm | 5 Gramm | 31,1 Gramm | 50 Gramm |
|---|---|---|---|---|
| Platin | 26,97 € | 134,85 € | 838,77 € | 1.348,50 € |
| Palladium | 26,92 € | 134,60 € | 837,21 € | 1.346,00 € |
Eigenschaften von Rhodium
Rhodium ist eines der sechs Platingruppenmetalle: Platin, Palladium, Rhodium, Osmium, Iridium und Ruthenium. Es wird auch als Edelmetall eingestuft, was bedeutet, dass es nicht so leicht mit Sauerstoff reagiert, als fantastischer Katalysator wirkt und resistent gegen Korrosion und Oxidation ist. Einige gemeinsame Eigenschaften der Platingruppenmetalle sind laut Chemie-Libretexten hohe Schmelzpunkte, allgemeine Ungiftigkeit und Beständigkeit gegen Verschleiß, Oxidation und Korrosion. Rhodium ist das Seltenste der Platingruppe und kommt nur bis zu einem Teil pro 200 Millionen in der Erdkruste vor, so Chemistry Libretexts. Rhodium hat eine geringere Dichte und einen höheren Schmelzpunkt als Platin. Laut Lenntech wird Rhodium von Luft und Wasser bis zu 1.112 Grad Fahrenheit (600 Grad Celsius) nicht angegriffen.
Rhodium in Zahlen
- Ordnungszahl (Anzahl der Protonen im Atomkern): 45
- Atomsymbol (im Periodensystem der Elemente): Rh
- Atommasse (mittlere Masse des Atoms): 102,90550
- Dichte: 12,41 Gramm pro Kubikzentimeter
- Phase bei Raumtemperatur: Fest
- Schmelzpunkt: 3.567 Grad F (1.964 Grad C)
- Siedepunkt: 6.683 Grad F (3.695 Grad C)
- Anzahl der Isotope (Atome desselben Elements mit einer unterschiedlichen Anzahl von Neutronen): 24, deren Halbwertszeiten bekannt sind; eines ist stabil
- Häufigste Isotope: Ein stabiles Isotop Rh-103
Preisentwicklung Edelmetalle seit 2012
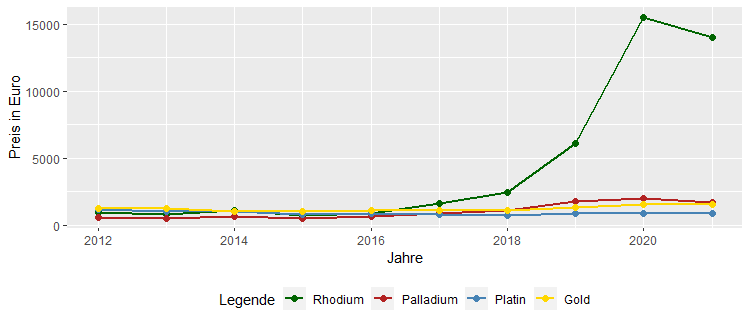
Bis zur Mitte der 2010er-Jahre waren die Edelmetallpreise auf einem gleichen Niveau. Trotz steigender Kurse bei Platin, Palladium und Gold hat sich der Rhodiumpreis seitdem erheblich positiver entwickelt. Es wurde teilweise eine Steigerung des Preises um den Faktor 15 Preises erreicht, sodass Rhodium mittlerweile im fünfstelligen Eurobereich je Unze Rhodium dotiert ist. Über mögliche Gründe für diesen signifikanten Preisanstieg gehen wir im Laufe des Textes genauer ein.
Entdeckung von Rhodium
Rhodium wurde 1803 vom englischen Chemiker William Hyde Wollaston entdeckt, kurz nachdem er das Element Palladium entdeckt hatte. Wollaston extrahierte Rhodium aus einem Stück Platinerz, das er in Südamerika gewonnen hatte. Rhodium kommt häufig mit Platinvorkommen vor und wird häufig bei der Gewinnung und Raffination von Platin gewonnen. Wollaston wurde erstmals von dem französischen Chemiker Hippolyte-Victor Collet-Descotils auf die Möglichkeit eines neuen Elements im Platinerz aufmerksam gemacht, der glaubte, dass die rote Farbe einiger Platinsalze auf das Vorhandensein eines nicht identifizierten Metalls zurückzuführen sei. Nach einer Reihe von chemischen Reaktionen gelang es Wollaston, das Platin und Palladium aus der Probe des Platinerzes zu entfernen. Zurück blieb ein dunkelrotes Pulver - das sich als Natriumrhodiumchlorid herausstellte.
Verwendungen von Rhodium
Das Hauptanwendungsgebiet von Rhodium sind Katalysatoren, die zur Reinigung von Autoabgasen dienen. Rhodium - oft zusammen mit Palladium und/oder Platin - erreicht dies durch die Reduzierung von Stickoxiden im Abgas. Ohne Rhodium-Katalysatoren wäre die Luft in unseren Städten durch Fahrzeugabgase viel schlechter. Da Rhodium sehr brillant und anlaufbeständig ist, wird es als Veredelung von Schmuck, Scheinwerfern und Spiegeln verwendet. Außerdem wird es in Legierungen mit Platin für Flugzeugturbinenmotoren verwendet. In der chemischen Industrie wird Rhodium nach Angaben der Royal Society of Chemistry (RSC) als Katalysator bei der Herstellung von Salpetersäure, Essigsäure und Hydrierungsreaktionen verwendet, außerdem zur Beschichtung von Glasfasern, Tiegeln, Thermoelementen und Scheinwerferreflektoren. Da es einen geringen elektrischen Widerstand hat und sehr korrosionsbeständig ist, wird es laut RSC auch als elektrisches Kontaktmaterial verwendet. Rhodium wird oft mit Platin und Iridium legiert, um ein oxidationsbeständiges Metall zu erhalten, das auch hohen Temperaturen standhält. Diese Legierungen werden in Ofenwicklungen, Schreibfedern, Phonographennadeln, Hochtemperatur-Thermoelement- und Widerstandsdrähten, Elektroden für Flugzeugzündkerzen, Lagern und elektrischen Kontakten verwendet.

Wer hätte das gedacht?
- Eine Legierung aus Rhodium-Platin wird in Herzschrittmachern verwendet.
- Rhodium ist gegen die meisten Säuren beständig.
- Rhodium-Metall wird selten allein und fast immer als Legierung verwendet.
- Von den drei Edelmetallen (Rhodium, Platin und Palladium), die der zeit in Fahrzeugkatalysatoren verwendet werden, hat Rhodium die bei weitem höchste Aktivität für die Entfernung von Stickoxiden (NOx) aus dem Abgas. Es hat auch eine sehr hohe Aktivität für die Oxidation von Kohlenwasserstoffen (HC) und Kohlenmonoxid (CO) und eine sehr gute Beständigkeit gegen die im Abgasstrom vorhandenen Gifte, so Eastern Catalytic. Sein größter Nachteil sind jedoch seine hohen Kosten.
- Alle Rhodiumverbindungen lassen sich leicht reduzieren oder durch Erhitzen zersetzen, um pulverförmiges (oder Schwamm-) Metall zu erzeugen.
Abbau von Rhodium
Kommerzielles Rhodium wird im Allgemeinen als Nebenprodukt der Kupfer- und Nickelraffination gewonnen. In der Natur kann Rhodium ungebunden oder mit anderen Platinmineralien vorkommen. Nach Angaben der Royal Society of Chemistry kann es in Flusssanden in Nord- und Südamerika und in Kupfer-Nickel-Sulfiderzen in Ontario, Kanada, gefunden werden. Aufgrund seiner Seltenheit, der geringen Marktgröße und des konzentrierten Angebots - Südafrika allein produziert etwa 80 Prozent des weltweiten Rhodiums - sind die Preise traditionel unbeständig.
Rhodium ist in der Lage Sonnenenergie zu speichern
Obwohl Rhodium eine solide Industrienische in der Reinigung von Autoabgasen gefunden zu haben scheint, zeigen viele neue Forschungsprojekte, dass das Edelmetall viel mehr Potenzial haben könnte, insbesondere in seiner primären Rolle als Katalysator. Durch einen neuen chemischen Prozess wird die Wärmeenergie der Sonne genutzt, um Kohlendioxid und Wasser in energiereiche Kraftstoffe umzuwandeln. Bei diesem chemischen Prozess kommt eine neue Materialkombination aus Ceroxid und geringen Mengen an Rhodium als Katalysator zum Einsatz. Diese Entdeckung von Schweizer Forschern ist ein großer Schritt in Richtung der chemischen Speicherung von Sonnenenergie (was für Wissenschaftler ein sehr kniffliges Problem war).

Was ist eine Rhodinierung und weitere Fragen?
Ein Metall hat mehr zu bieten als seine Farbe. Deshalb ist die Wahl zwischen rhodiniertem Silber, Sterlingsilber oder Weißgold keine leichte Aufgabe. Sie haben alle eine silberne Farbe, aber der Unterschied liegt in der Haltbarkeit, dem Glanz und den Kosten. Wenn Sie einen hochwertigen Ring, eine Halskette oder Ohrringe in einem strahlenden Weiß suchen, das das Licht einfängt, dann ist rhodinierter Schmuck die beste Wahl. Die Rhodinierung bietet Schutz vor harten Stößen und bringt die umliegenden Edelsteine zum Leuchten.
WAS IST RHODIUM?
Rhodium ist das weißeste und wertvollste Metall, das für Schmuck verwendet wird. Es ist seltener als Gold oder Platin und weißer als Silber. Das Metall kommt so selten vor, dass es meist als Nebenprodukt von Platinminen gewonnen wird. Rhodium gehört zur gleichen Gruppe von Metallen wie Platin (Platingruppe), zu der Platin, Rhodium, Iridium, Ruthenium, Osmium und Palladium gehören. Sein extremer Glanz, sein Reflexionsvermögen und seine Festigkeit machen Rhodium zu einem begehrten Material für die Automobil-, Beleuchtungs- und Spiegelindustrie sowie für die Schmuckherstellung.
WAS BEDEUTET RHODINIERT?
Rhodinierter Schmuck besteht aus einem Basismetall (Gold, Silber oder eine andere Legierung), das mit einer dünnen Rhodiumschicht überzogen ist, um ihm zusätzliche Festigkeit und Glanz zu verleihen. Mit Rhodium beschichteter Schmuck ist glänzender und haltbarer als andere Metalle. Die Rhodiumbeschichtung verkratzt, verbeult oder korrodiert nicht und behält ihren Glanz.
WELCHE FARBE HAT RHODIUM?
Rhodium ist ein leuchtendes, silberweißes und stark reflektierendes Material. Wegen seines Glanzes und seiner Qualität ziehen viele Juwelliere es vor, ihre Schmuckstücke mit Rhodium zu beschichten, anstatt sie mit Weißgold oder Platin zu gestalten.
WARUM WIRD SCHMUCK RHODINIERT UND WAS SIND DIE VORTEILE?
Rhodinierter Schmuck verleiht dem Schmuck eine zusätzliche Schutzschicht und erzeugt ein helleres Weiß als Sterlingsilber, Weißgold oder Platin. Realistisch betrachtet kann Schmuck nicht aus massivem Rhodium hergestellt werden, da Rhodium trotz seiner Stärke spröde ist. Eine Rhodiumschicht muss genau die richtige Dicke haben, damit sie nicht bricht - 0,75-1,0 Mikrometer sind die optimale Stärke. Bei einer dünneren Schicht würde das darunter liegende Metall durchscheinen, bei einer dickeren Schicht würde die Beschichtung reißen. Diese perfekte Rhodiumschicht kann das Aussehen, die Qualität und die Langlebigkeit Ihres Schmucks verbessern.
IST RHODIUM HYPOALLERGEN?
Rhodium ist hypoallergen, da es kein Nickel enthält, das schwere Hautreaktionen hervorrufen kann. Es schützt vor anderen Metallen, die mit Nickel legiert sind, um Ihre Haut zu schützen. Wenn Sie eine Nickelallergie haben oder einfach nur Ihre Haut schützen wollen, ist Rhodium eine ausgezeichnete Option.
IST RHODIUMSCHMUCK SICHER ZU TRAGEN?
Auf jeden Fall. Rhodium ist ungiftig und absolut sicher. Es ist die empfohlene Wahl für empfindliche Haut, Babys und neue Piercings. Da Rhodium nickelfrei ist, reizt es die Ohren nicht und hinterlässt keine Hautausschläge.
LÄUFT RHODIUM AN?
Rhodium ist nickelfrei und läuft daher nicht an. Rhodium ist außerdem korrosionsbeständig und rostet nicht. Da Rhodium stark ist, muss es nicht mit anderen Metallen wie Nickel oder Kupfer legiert werden, die mit der Zeit korrodieren und dunkelgrüne Flecken auf der Haut hinterlassen.
WAS IST RHODINIERTES STERLINGSILBER?
Rhodiniertes Silber ist Sterlingsilber, das mit Rhodium beschichtet ist, um es weißer und heller zu machen. Da Silber ein weicheres Metall ist, wird es durch Rhodium vor Kratzern und Abnutzung geschützt. Massives Silber ist zu weich, um zu Schmuck verarbeitet zu werden. Es besteht daher zu 92,5 % aus Silber und zu 7,5 % aus anderen Metallen wie Kupfer, Nickel oder einer Kombination aus beidem. Die Spuren von Kupfer und Nickel in Sterlingsilber führen zum Anlaufen. Eine Rhodiumbeschichtung verhindert dies.
VERGLEICH VON RHODIUM UND SILBER
Silber ist nicht so weiß und reflektierend wie Rhodium. Es ist weicher und muss mit anderen Metallen kombiniert werden, die es anfällig für Anlaufen machen. Sterlingsilber wird oft als Basismetall für Rhodium verwendet, da es robust und hochwertig ist. Rhodium verleiht dem Silber einen gewissen Wert und Unvergänglichkeit.
WAS IST BESSER, RHODINIERTES ODER STERLINGSILBER?
Ob Sie rhodinierten oder Sterlingsilberschmuck bevorzugen, ist eine Frage der Vorliebe. Rhodinierter Schmuck und Schmuck aus Sterlingsilber lassen sich am besten miteinander kombinieren. Sterlingsilber enthält Nickel und Kupfer und läuft mit der Zeit an und färbt Ihre Finger schwarz. Mit einer Rhodiumschicht überzogen, wird Silber jedoch zu einem besseren Metall. Rhodium schützt Ihre Haut vor dem geringen Anteil an Neusilber und beseitigt das Risiko des Anlaufens. Wenn sich die Rhodiumbeschichtung abnutzt, ist dies bei Silber nicht so offensichtlich, da beide Metalle eine ähnliche Farbe haben. Das bedeutet, dass Sie zwischen den einzelnen Beschichtungen möglicherweise länger warten können.
VERGLEICH VON RHODIUM UND PLATIN
Sowohl Rhodium als auch Platin sind silberne Edelmetalle und gehören zur gleichen Metallgruppe. Rhodium wird zusammen mit Platin gewonnen, und beide Metalle sind selten und wertvoll. Rhodium ist sogar noch seltener als Platin und hat einen viel höheren Preis. Aber wenn die Dicke von Rhodium 1,0 Mikrometer überschreitet, wird es spröde, so dass ein Juwelier kein Schmuckstück ganz aus Rhodium herstellen kann. Platin ist verformbarer und bricht nicht, wenn es dick ist. Es wird für Schmuckstücke verwendet, die leicht zu pflegen und langlebig sind. Platinschmuck ist jedoch teurer als rhodinierter Schmuck, auch wenn das Metall selbst weniger wertvoll ist. Rhodium-Schmuck hat nur eine dünne Beschichtung aus feinem Metall, was ihn erschwinglicher macht, aber genauso schön und sogar reflektierender als Platin.
VERGLEICH VON RHODIUM UND GOLD
Die Farbe ist der offensichtlichste Unterschied zwischen Rhodium und Gold. Gold hat einen warmen gelben Farbton, während Rhodium ein kühles Silber ist. Beide Metalle sind langlebig, wertvoll und teuer. Schmuck kann aus massivem Gold hergestellt werden, ebenso wie aus Platin, während Rhodium nur zur Beschichtung anderer Metalle verwendet wird. Wenn Sie Ihren Goldschmuck nicht versilbern wollen, ist die Beschichtung von Gelbgold mit Rhodium nicht zu empfehlen. Mit der Zeit wird das Gold durch das Rhodium durchscheinen. Vor der Rhodiumbeschichtung wird Gold oft gebleicht und durch die Kombination mit anderen Metallen weiß gemacht.
VERGLEICH RHODIUMPREIS UND GOLDPREIS
Die Kosten für Rhodium sind je nach Markt doppelt so hoch oder höher als für Gold. Massiver Goldschmuck ist teurer als rhodinierter Schmuck, aber beide sind von hoher Qualität.
RHODINIERTES WEISSGOLD
Der meiste Weißgoldschmuck auf dem Markt ist rhodiniert. Wenn Ihr "Weißgold"-Schmuck silberglänzend ist, hat er wahrscheinlich eine Rhodiumschicht. Wenn er einen leichten Gelbstich hat, handelt es sich wahrscheinlich um echtes Weißgold. Der Besitz von rhodiniertem Weißgold ist jedoch nicht schlecht - die Rhodiumbeschichtung erhöht den Wert und die Haltbarkeit. Sie müssen sich nur auf eine gewisse Pflege einstellen, damit der reflektierende Glanz erhalten bleibt. Massives Weißgold ist nicht weiß, sondern leicht gelblich. Durch die Rhodinierung von Weißgold wird dieser Gelbstich beseitigt. Unterschiedliche Goldtöne entstehen durch das Legieren oder Kombinieren von Metallen. Bei der Herstellung von Weißgold wird häufig Nickel als Bleichmittel zugesetzt. Eine Rhodiumschicht schützt Ihre Haut vor dem Kontakt mit dem Nickel im Weißgold.
WIE LANGE HÄLT EINE RHODIUMBESCHICHTUNG?
Im Durchschnitt hält eine Rhodiumbeschichtung ein Jahr lang. Bereiten Sie sich darauf vor, Ihren Schmuck jährlich erneuern zu lassen. Wie lange rhodinierter Schmuck hält, hängt jedoch von der Häufigkeit der Reibung ab, der er ausgesetzt ist. Ansonsten ist das Metall extrem haltbar. Wenn Sie Ihren rhodinierten Schmuck täglich tragen, muss er möglicherweise nach 6 Monaten erneuert werden. Wenn Sie Ihren rhodinierten Schmuck jedoch für besondere Anlässe aufbewahren, können Sie unter Umständen mehrere Jahre warten, bevor Sie ihn erneuern. Ob Ihr Rhodiumschmuck erneuert werden muss, erkennen Sie am besten, indem Sie ihn mit dem Auge betrachten. Wenn Sie das unedle Metall durch das Rhodium hindurch sehen können, ist es an der Zeit, es zu erneuern. Wann die Rhodiumbeschichtung ersetzt werden sollte, hängt auch von der Art des Schmucks ab. Ein rhodinierter Ring nutzt sich schneller ab als eine rhodinierte Halskette, es sei denn, Sie tragen die Halskette häufiger als den Ring.
WIE REINIGT MAN RHODINIERTES STERLINGSILBER?
Es empfiehlt sich, Ihren rhodinierten Schmuck nicht regelmäßig zu reinigen, da er sich durch Reiben schneller abnutzt. In der Regel wird er nicht anlaufen. Wenn Sie ihn dennoch reinigen möchten, sollten Sie Seife, Wasser und auf jeden Fall scharfe Chemikalien vermeiden. Verwenden Sie außerdem ein Material zum Abwischen, das nicht zu viel Reibung erzeugt. Wenn Ihr Rhodiumschmuck seinen Glanz verloren hat, ist er wahrscheinlich abgenutzt und es ist Zeit, ihn zu erneuern. Warten Sie so lange wie möglich, bevor Sie ihn erneuern, denn häufige Pflege kann das Grundmetall abnutzen.
PFLEGE IHRES RHODINIERTEN SCHMUCKS
- Vermeiden Sie Wasser, Seife und scharfe Chemikalien. Ein wenig Wasser schadet nicht, aber Sie müssen ihn wahrscheinlich abtrocknen, was die Reibung erhöht.
- Vermeiden Sie es, rhodinierte Schmuckstücke an- und abzulegen. Viele Menschen haben die Angewohnheit, ihre Halsketten zu verdrehen oder Ringe an ihren Fingern hinauf- und hinunterzuschieben. Achten Sie darauf, nicht mit Ihrem rhodinierten Schmuck herumzuhantieren, damit er möglichst lange hält.
- Versuchen Sie, rhodinierten Schmuck für besondere Anlässe zu reservieren, um ihn zu erhalten. Tragen Sie ihn auf keinen Fall bei der Haus- oder Gartenarbeit oder im Fitnessstudio.
KOSTEN EINER RHODINIERUNG?
Das Erneuern von Rhodium kostet zwischen etwa 30,00 bis 100,00 Euro. Das ist abhängig von der Preiskalkulation des Goldschmieds. Eine Rhodinierung ist nicht zeitaufwendig, aber ein komplizierter Prozess. Rhodium ist teurer als jedes andere Metall, aber eine Rhodiumbeschichtung ist weniger kostspielig als massives Gold oder Platin. Der Preis Ihres rhodinierten Schmucks hängt vom Wert des Grundmetalls ab. Wäre es möglich, einen Ring aus massivem Rhodium herzustellen, wäre er unglaublich teuer.
LOHNT SICH EINE RHODIUMBESCHICHTUNG?
Ob sich eine Rhodinierung lohnt, hängt davon ab, welches Aussehen Sie wünschen und wie viel Sie investieren möchten. Die Rhodinierung ist eine preiswertere Alternative zu Gold oder Platin, erfordert aber eine gewisse Pflege.
VORTEILE VON RHODIUMBESCHICHTUNGEN
- Verleiht dem Schmuck eine schöne Optik
- Langlebig
- Hochwertig
- Hypoallergen
- Ungiftig
NACHTEILE DER RHODIUMBESCHICHTUNG
- Gewisse Pflege erforderlich
- Nutz sich je nach Beanspruchung ab und das Grundmaterial tritt zum Vorschein
- Sollte nicht zu starker Sonneneinwirkung ausgesetzt werden

Fazit zu Rhodium
Rhodium ist das teuerste Metall der Welt, sogar noch teurer als Gold oder Platin, und es ist extrem selten. Es ist hypoallergen, extrem glänzend, korrosionsbeständig und äußerst langlebig. Aufgrund all dieser Eigenschaften eignet sich Rhodium hervorragend für die Herstellung von Schmuck, aber wegen der Härte und Sprödigkeit des Metalls sowie der exorbitanten Kosten kann es nicht in seiner reinen Form für die Schmuckherstellung verwendet werden.
Die einzige Möglichkeit, Rhodium für Schmuck zu verwenden, ist die Beschichtung anderer Metalle wie Gold, Platin, Messing, Silber und Palladium, um nur einige zu nennen. Bei einer Rhodinierung wird mit Hilfe eines galvanischen Verfahrens auf Sterlingsilber aufgebracht. Der gereinigte Silberschmuck wird in ein Bad mit einer Rhodiumlösung gelegt. Mit Hilfe von positivem elektrischem Strom wird das Rhodium dann dauerhaft auf dem Silber fixiert.